LA PROTEZIONE CATODICA
Fondamenti Teorici1. La corrosione dei metalli
La corrosione dei metalli è un fenomeno fisico-chimico che avviene con degradazione di uno o più metalli in contatto con un certo ambiente e che comporta la presenza simultanea di due reazioni, una anodica di ossidazione e una catodica di riduzione.
Quando un metallo è a contatto con un elettrolita (acqua, terreno, umidità, ecc.) assume un potenziale elettrico determinato dalle reazioni chimiche citate ed il cui valore dipende dal metallo e dall’elettrolita. Due metalli diversi a contatto elettrico fra loro e immersi in un elettrolita, assumendo due diversi valori di potenziale, provocano il flusso di una corrente elettrica spontanea che tende a condurre i potenziali naturali dei metalli verso uno stesso valore detto potenziale di corrosione o misto. La circolazione di corrente nel metallo avviene a livello elettronico, mentre nell’elettrolita avviene mediante migrazione ionica connessa con le reazioni di ossidoriduzione e pertanto con disgregazione del metallo il cui potenziale è più anodico.
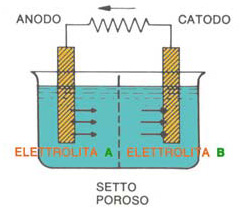
Pila elettrica costituita da due elettrodi dello stesso metallo immersi in due elettroliti diversi.
2. La protezione catodica
Fornendo alla coppia di metalli presa in considerazione al punto precedente una corrente elettrica esterna, provochiamo una variazione del potenziale misto introducendo forzatamente una sovratensione. È dimostrabile che, se questa sovratensione è tale da provocare una diminuzione del potenziale misto fino ad un valore inferiore al potenziale del metallo più anodico, non può più avvenire la reazione di corrosione. Su questo concetto, scoperto nel 1824 da Humphry Davy, si basa la protezione catodica, che consiste appunto nel rendere la superficie di un metallo da proteggere più elettronegativa di quello che è il suo potenziale di ossidoriduzione in un determinato elettrolita. Naturalmente la corrente deve essere fornita realizzando un circuito in grado di far circolare la corrente nell’elettrolita con scambio ionico alimentato da una reazione di ossidazione. In altre parole, non sarà sufficiente disporre di un generatore di corrente elettrica continua, ma sarà necessario inserire nel circuito anche un elemento sacrificabile su cui possa avvenire la reazione di ossidazione.
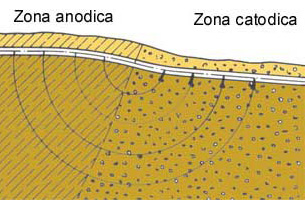
Pila geologica.
3. Protezione catodica con alimentatori
In questo caso la corrente elettrica viene fornita da un alimentatore costituito essenzialmente da un trasformatore e da un raddrizzatore di corrente. Al polo negativo nell’alimentatore è collegata la struttura metallica da proteggere, mentre al polo positivo viene collegato il «dispersore» che ha lo scopo di assicurare la corrente nell’elettrolita. Il dispersore ovviamente dovrà essere posato nello stesso ambiente in cui si trova la struttura da proteggere.
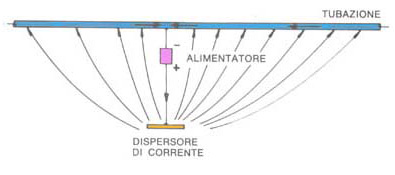
Protezione catodica con alimentatore.
4. Protezione catodica con anodi galvanici
Questo metodo sfrutta la corrente stessa di corrosione per ottenere un potenziale di protezione per la struttura interessata. Per ottenere ciò bisogna collegare al metallo da proteggere un altro elemento costituito da un metallo sicuramente più anodico del precedente e tale per cui il potenziale misto che si viene a realizzare sia più elettronegativo del potenziale di protezione richiesto. È chiaro che un anodo galvanico deve avere un potenziale molto più anodico di quello del metallo da proteggere e deve inoltre essere in grado di liberare una elevata quantità di ioni per assicurare una adeguata circolazione di corrente.
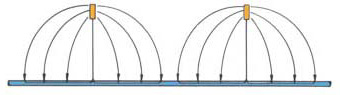
Protezione catodica con anodi galvanici.
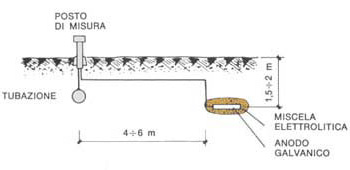
Esempio di installazione di anodo galvanico.
5. Dimensionamento di un impianto di protezione catodica
Per la determinazione dei valori di corrente da fornire e del potenziale di struttura (d.d.p.) da imporre è necessario conoscere tramite misure preliminari e prove di alimentazione i parametri caratterizzanti le strutture da proteggere. I valori da ricavare sono i seguenti: R = resistenza longitudinale Va = ddp ad alimentatore inserito Vs = ddp ad alimentatore disinserito Vn = ddp naturale Vr = Resist. isol. x I = Va-Vs Vp = polarizzazione = Vs-Vn In base ai valori ricavati è possibile determinare la resistenza di isolamento della struttura che è data da: Ris = Variazione di potenziale x Superficie/corrente fornita. Le tensioni sono in Volt, le correnti in Ampere e le resistenze in Ohm. Bisogna eseguire anche misure della resistività dei terreni sia alla profondità di posa delle strutture che alla profondità e nelle ubicazioni ipotizzate per la posa dei dispersori anodici.
Per le misure della resistività in superficie si impiegano quattro aste metalliche (elettrodi) lunghe circa 500 mm, con diametro di circa 10 mm. Esse vengono infisse nel terreno a distanze eguali secondo un allineamento rettilineo e collegate ad un misuratore di resistenza a quattro morsetti alimentato da un generatore a corrente alternata di frequenza opportuna.
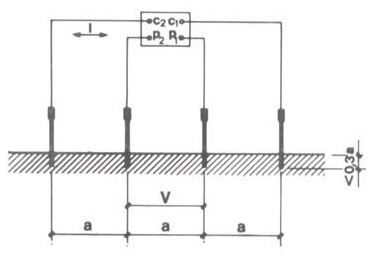
Misura della resistività del terreno con il metodo (Wenner) dei quattro elettrodi in superficie.
Si richiama l’attenzione sul fatto che la presenza di strutture metalliche interrate può alterare i risultati della misura. Pertanto in presenza di condutture metalliche interrate può, ad es., essere opportuno realizzare un allineamento perpendicolare al tracciato delle stesse, sistemando tutti gli elettrodi dallo stesso lato rispetto alla condotta.
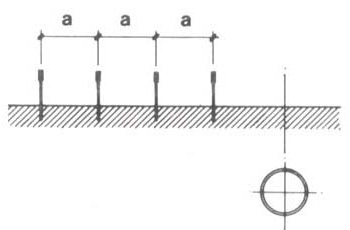
Disposizione degli elettrodi nel caso di presenza di una struttura interrata.
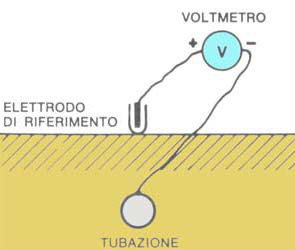
Misura del potenziale istantaneo di una tubazione.
5a – Determinazione della corrente di protezione.
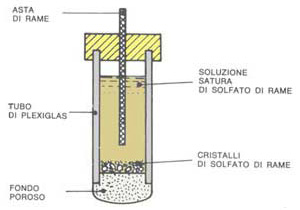 Sulla base del valore di resistenza di isolamento sopra ricavato, si calcola la corrente necessaria per la protezione catodica della struttura, imponendo che nei punti più sfavoriti la d.d.p. verso terra sia almeno —0.9 V, ma mai più negativa di —2 V con riferimento all’elettrodo impolarizzabile al solfato di rame.
Sulla base del valore di resistenza di isolamento sopra ricavato, si calcola la corrente necessaria per la protezione catodica della struttura, imponendo che nei punti più sfavoriti la d.d.p. verso terra sia almeno —0.9 V, ma mai più negativa di —2 V con riferimento all’elettrodo impolarizzabile al solfato di rame.
Per determinare la corrente, si devono prima determinare i valori della resistenza unitaria R di isolamento pari al rapporto fra la resistenza di isolamento e la superficie unitaria esterna, e quindi la costante di attenuazione alfa data dalla radice quadrata del rapporto fra la resistenza longitudinale e la resistenza unitaria. Una volta nota la costante di attenuazione è possibile determinare la corrente e la d.d.p. nel punto di alimentazione mediante le formule di attenuazione:
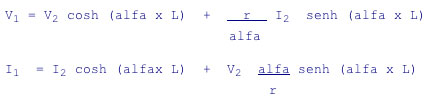
I valori di d.d.p. da assumere nei punti estremi per i calcoli saranno relativi alla sola tensione prodotta dalla circolazione della corrente, con esclusione del potenziale naturale e della polarizzazione.
5b – Calcolo dei dispersori
Il peso di ciascun dispersore è dato dalla formula ![]() dove:
dove:
- I è la corrente da erogare
- Cons. è il consumo in Kg. per A. anno
- rend. è il rendimento delle barre costituenti il dispersore.
5c – Calcolo della potenza elettrica da installare
La resistenza che entra in gioco nel circuito elettrico formato dall’alimentatore, dal dispersore, dal terreno e dalla struttura è valutabile come somma delle singole resistenze:
- Rd = resistenza del dispersore
- Rt = resistenza equivalente della struttura
- Rc = resistenza dei cavi elettrici.
La resistenza di un dispersore posato in verticale è ![]() dove:
dove:
- res è la resistività del terreno in Ohm.cm
- N il numero di elementi che compongono il dispersore
- L la lunghezza degli elementi in cm
- S la spaziatura fra gli elementi.
La resistenza equivalente della struttura si può ricavare con la formula ![]() dove L è la lunghezza della struttura. La resistenza dei cavi, supponendo che in un impianto ad alimentatore si utilizzino circa 100 m di cavo con sezione 16 mmq, è di circa 0.1 ohm. La potenza elettrica necessaria in corrente continua è
dove L è la lunghezza della struttura. La resistenza dei cavi, supponendo che in un impianto ad alimentatore si utilizzino circa 100 m di cavo con sezione 16 mmq, è di circa 0.1 ohm. La potenza elettrica necessaria in corrente continua è ![]() in corrente alternata è
in corrente alternata è ![]() Il consumo annuo di corrente previsto è
Il consumo annuo di corrente previsto è ![]()
La Protezione Catodica è una tecnica elettrochimica di salvaguardia dalla corrosione di strutture metalliche esposte a un ambiente elettrolitico (terreni, acqua marina, acqua dolce, sostanze chimiche, ecc.) che può essere aggressivo nei confronti del metallo.
Al link sottostante sono disponibili programmi gratuiti per il calcolo del valore dell’indicatore di Protezione Catodica Kt, in accordo a quanto prescritto dalle relative linee guida elaborate dall’APCE e pubblicate dall’UNI.
Associazione per la Protezione dalle Corrosioni Elettrolitiche
